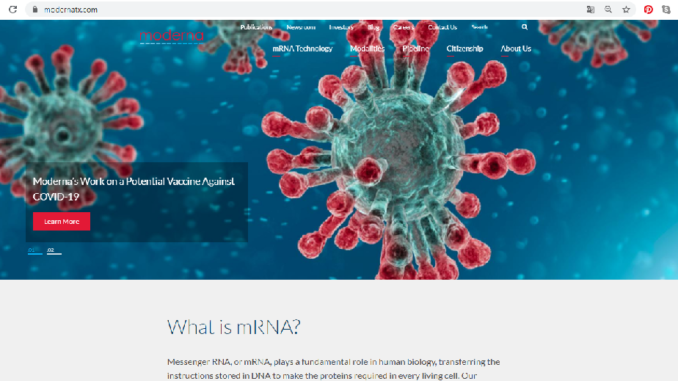
La primera vacuna probada en humanos para luchar contra el SARS-CoV-2 obtuvo resultados «positivo» en una primera fase de su experimentación y demostró «potencial para evitar la enfermedad de COVID-19», informó este lunes Moderna Inc., un biofamarceútica estadounidense.
Portavoces de la firma han avanzado que, si las siguientes fases siguen este camino, la futura vacuna denominada mRNA-1273 podría estar disponible en Estados Unidos a finales de año y a nivel internacional a principios de 2021.
La farmacéutica con sede en Cambridge (Massachusetts, EE.UU.) es una de las ocho firmas a nivel global que están desarrollando ensayos clínicos en humanos de una vacuna contra el nuevo coronavirus. Ésta se basa en una tecnología propia a partir de la inoculación de proteínas que deben generar la inmunidad, dando al cuerpo instrucciones genéticas contra el virus.
Esta vacuna debe provocar una respuesta inmunitaria tan potente como la de los pacientes que han superado la enfermedad gracias a anticuerpos neutralizantes.
PRIMER ENSAYO CON 45 PERSONAS
«Los datos provisionales de la Fase 1, aunque tempranos, demuestran que la vacuna con mRNA-1273 desarrolla una respuesta inmune de la magnitud causada por la infección natural, empezando con una dosis tan baja como 25 microgramos», dijo en una nota el jefe médico de Moderna Inc., Tal Zaks.
Los 45 adultos, entre hombres y mujeres de 18 a 55 años sanos que participaron en el estudio dirigido por el Instituto Nacional de Alergias y Enfermedades Infecciosas (NIAD, en inglés), fueron separados en tres grupos a los que se les administró diferentes dosis, de 25, 100 y 250 microgramos.
La vacuna fue «generalmente segura y bien tolerada» por los participantes, que desarrollaron anticuerpos contra el COVID-19, pero Moderna destaca los resultados en los grupos que recibieron dos dosis de 25 y 100 microgramos.
En el día 43 del estudio, dos semanas después de que se les inyectara la segunda dosis a los participantes del grupo de 25 microgramos, «los niveles de anticuerpos vinculantes estaban en los niveles vistos en sérum convalesciente (muestras de sangre de personas que se han recuperado del COVID-19)».
Los participantes de grupo que recibió dos dosis de 100 microgramos «excedían» esos niveles de anticuerpos vistos en el sérum convalesciente, destaca la nota.
La firma señaló que su vacuna experimental «desarrolló anticuerpos neutralizadores» en ocho participantes procedentes de esos dos grupos, cuatro de cada y los únicos de los que tiene datos, de momento.
Ahora la biotecnológica prosigue con la Fase 2, aprobada por el regulador estadounidense a principios de este mes y en la que participarán unas 600 personas, mientras que después planea una Fase 3 con miles de participantes para este mes de julio cuyo objetivo es confirmar los resultados de las etapas previas.
PRIMERA PRODUCCIÓN EN MASA
Paralelamente al desarrollo, Moderna realiza preparativos a gran escala para la producción en masa.
Acaba de anunciar un contrato de 10 años con la compañía farmacéutica suiza Lonza para producir la vacuna. Con el apoyo financiero de la Agencia de los Estados Unidos para la Investigación Biomédica Avanzada (BARDA), el sistema de producción de vacunas se establecerá en base a la fabricación de Lonza en los Estados Unidos y Suiza.
El primer envío se espera en julio y el objetivo es asegurar una capacidad de producción de mil millones de dosis al año a partir de 2021.
«Continuaremos desarrollándonos al ritmo más rápido posible mientras garantizamos la seguridad», dijo Stephen Banssel, CEO de Moderna.
OFERTA DE ACCIONES PARA FINANCIAR LA VACUNA
Tras toda esta información, Moderna se disparó un 19,96 % en el Nasdaq y en algunos momentos de la hornada hasta un 30 %, ayudando a una jornada optimista en Wall Street. En los últimos tres meses, su valor de mercado ha aumentado un 340 %.
La farmacéutica aprovechó el tirón y este mismo lunes anunció una oferta pública de acciones por valor de 1.250 millones de dólares para financiar la posible fabricación y comercialización de la vacuna. AGENCIAS
Descubre más desde International Press - Noticias de Japón en español
Suscríbete y recibe las últimas entradas en tu correo electrónico.
























Be the first to comment